- introduzione
- l'energia, 1° parte
- l'energia, 2° parte
- l'energia, 3° parte
- l'energia, 4° parte
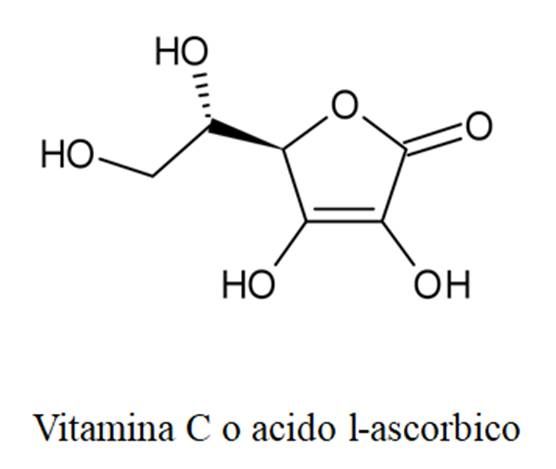
- Vitamine cotte?
- Croste dorate
- caramellizzazione
- Cuocere il pane - 1
- cuocere il pane - 2
- cuocere il pane - 3
- pane raffermo
- riso e pasta
- l'amido
- i carboidrati
- microonde e fesserie
- cuocere con la radio
- cuocere a freddo - 1
- cuocere a frustate
- salatura
- cottura e reni
- il sale nell'acqua!
- colore e cottura
- patatine fritte
- oli di frittura 1
- oli di frittura - 2
- santa frittura!
- arrosto
- bollito
- cuocere=ammorbidire
- uova avide
- cuocere le uova
- mangiare proteine
- le proteine
- arrosti pericolosi
- arrosti di carne
- cuocere i pomodori
- perché cuocere
- fagioli assassini
- cuocere i funghi